より優れたパルス・オキシメータの設計
概要
利便性が高く、消費電力の少ない医療用機器を実現するのは、従来にも増して重要なことになっています。本稿では、まずSpO2(Peripheral Blood Oxygen Saturation:経皮的動脈血酸素飽和度)の測定方法について説明します。その上で、優れたパルス・オキシメータを実現するために、新世代の光学アナログ・フロント・エンド(AFE)がどのように貢献するのか解説します。そうしたAFE製品を採用することで、設計の複雑さや機械的な設計に費やさなければならない負担を軽減し、消費電力を低減することが可能になります。
はじめに
従来、SpO2の測定は指や耳といった身体の末梢部で行っていました。最も一般的な方法は、クリップ式の機器を使ってヘモグロビンの総量に対する酸素飽和ヘモグロビンの比を測定するというものです。それによって得られる測定値は、赤血球が酸素を肺から身体の他の部分にどの程度うまく運ぶことができているかということを表します。健康な成人の場合、正常なSpO2のレベルは95%~100%となります。SpO2の値が上記の値を下回る場合には、低酸素血症と呼ばれる状態であるということになります。これは、健康な臓器や認知機能を維持するために必要な量の酸素が身体に送り届けられていないということを意味します。
低酸素血症を発症すると、めまい、錯乱、息切れ、頭痛などの症状が現れます。また、何らかの病状が原因でSpO2が低下することもあります。自宅や臨床の現場で連続的/断続的にSpO2をモニタリングすれば、そうした事態を避けることができます。
SpO2は、臨床の現場で記録される非常に一般的なバイタル・サインの1つです。SpO2の連続的なモニタリングを必要とする疾患としては、喘息、心臓病、COPD(慢性閉塞性肺疾患)、肺疾患、肺炎、そしてCOVID-19(新型コロナウイルス感染症)によって生じる低酸素症などが挙げられます。
COVID-19の患者については、入院が必要であるか否かを判断しなければなりません。その方法の1つは、SpO2をモニタリングすることです。SpO2のレベルが基準値を下回っている場合(通常92%未満)、その患者は緊急治療室に入る必要があります。
COVID-19と低酸素症の関係
COVID-19についての分析が進んだ結果、患者には「静かな低酸素症」として知られる潜行性の高い症状が現れることがわかりました。その症状は、息切れのような呼吸器に関するCOVID-19の典型的な症状が現れる前の段階で、身体に深刻なダメージを与える可能性があります。米国立バイオテクノロジー情報センターのウェブサイトには、「COVID-19による肺炎が危険なレベルに進行するのを防ぐためには、患者が息切れを感じ始める前に、無症候性の低酸素症を検出できるようにすることが非常に重要である」と記載されています1。
また、SpO2のモニタリングは、睡眠時無呼吸症候群の診断を行う上でも重要な指標になります。閉塞性の症状が現れている場合、睡眠中に気道が部分的あるいは完全に塞がれてしまいます。これは、呼吸が長時間休止している、あるいは呼吸が浅くなっている期間として観測されます。その場合、一時的な低酸素症を引き起こしているはずです。この症状を長期間放置していると、心臓発作、脳卒中、肥満の可能性が高まることがあります。発症者の数は、全成人人口の1%~6%に達すると推定されています。
優れたパルス・オキシメータの実現が急務に
患者のモニタリングについては、携帯型の機器によって行ったり、在宅で行えるようにしたりすることが求められています。言い換えれば、ユーザが日常生活を送る上で邪魔にならないVSM(Vital Sign Monitoring)機器の開発が急務になっています。SpO2については、指や耳以外の部位でモニタしようとすると、計測システムの設計に多くの課題が生じます。しかし、無症候性の低酸素症に注目が集まったこともあり、携帯性の高い医療グレードのパルス・オキシメータの開発がより一層切実なニーズになっています。
以下では、まずSpO2の計測に使用される基本的な原理について説明します。その上で、SpO2の計測に使用される医療グレードの機器の設計方法について解説します。特に、その種の機器の設計に役立つ製品として、アナログ・デバイセズが提供する光学測定向けのAFE「ADPD4100/ADPD4101」を紹介します。これらの製品を利用すれば、SpO2の計測システムを設計する際の複雑さを軽減することができます。例えば、周辺光を自動的に除去する機能を備えていることから、機械的/電気的な設計における負担を軽減することが可能です。ADPD4100は、消費電力が少なくダイナミック・レンジが広いことを特徴とします。そのため、フォトダイオード(PD)の数やLEDに流す電流を削減することができます。しかも、SpO2のわずかな変化を高い効率で検出可能なシステムを構築できます。また、オプションのデジタル積分器を使用すると、極めて効率が高く消費電力の少ない動作モードを選択できます。その結果、光の信号パスに存在するアナログ・ブロックの動作を停止することにより、可搬型の光電式容積脈波記録法(PPG:Photoplethysmography)システムの稼働時間を延伸することが可能になります。
酸素飽和度とは何か?
血液中のヘモグロビンの総量に対する酸素飽和ヘモグロビンの割合のことを酸素飽和度(Oxygen Saturation)と呼びます。酸素飽和度の絶対的な基準として使われているのは、動脈血酸素飽和度(SaO2)です。但し、SaO2を計測するには、血液のサンプルを取得し、実験室においてガス分析を行わなければなりません(これについては、後ほど触れます)。
SpO2は、パルス・オキシメータを使って身体の周辺部で計測した酸素飽和度の推定値です。最近まで、酸素飽和度の最も一般的な測定方法は、指に装着したパルス・オキシメータを使用するというものでした。
パルス・オキシメータの動作原理
酸化ヘモグロビン(HbO2)と還元ヘモグロビン(RHb)とでは、特定の波長における光の吸収量が大きく異なります。パルス・オキシメータは、この原理に基づいて動作します。図1に、HbO2、ヘモグロビン(Hb)、メトヘモグロビン(MetHb)の吸光係数を示しました。吸光係数は、化学物質が特定の波長の光をどれだけ吸収するのかを示す値です。図1の周波数スペクトルは、可視光域と赤外光域を網羅しています。これを見ると、HbO2はより多くの赤色光(600nm)を吸収し、より多くの赤外光(940nm)を透過することがわかります。一方、RHbはより多くの赤外光を吸収し、HbO2よりも多くの赤色光を透過することが見てとれます。
最も基本的なパルス・オキシメータは、反射型または透過型に構成にした2個のLEDと1個のPDから成ります。LEDとしては、660nmの赤色LEDと940nmの赤外光(IR)LEDを各1個使用します。パルス・オキシメータでは、赤色LEDを時間軸で見てパルス状に発光させ、PDに生じた信号を測定します(図2)。また、それと同じことを、赤外光LEDを使って行います。最後に、両LEDをオフにし、外部光源(周辺光)に対する測定を行ってベースラインを取得します。そのようにして、両方の波長に対応するPPGの信号を取得します。


図1. ヘモグロビンを通った光の吸光係数


図2. パルス・オキシメータの基本的な回路構成
そのPPG信号には、DC成分とAC成分が含まれています。DC成分は、皮膚、筋肉、骨、静脈血といった反射物によって生じます。一方のAC成分は、体動(身体の動き)が少ない場合、主に動脈血の脈動からの反射光によって構成されます。また、AC成分は心拍数と動脈の厚さに依存します。反射光/透過光は、拡張期(弛緩)よりも収縮期(送り出し)に多くなります。収縮期には、心臓から血液が送り出され、動脈圧が上昇します。血圧が上昇すると動脈が拡張し、動脈血の体積が増加します。このようにして血液が増えることにより、光の吸収量が増加します。拡張期には血圧が低下するので、光の吸収量も減少します。図3は、心臓の拍動で生じる拡張期の谷と収縮期のピークを示したものです。


ランベルト‐ベールの法則によると、光はそれを吸収する物質中を通過する際に指数関数的に減衰します。この法則を利用すると、ヘモグロビンの総量に対するHbO2のレベルを算出することができます。
拡張期と収縮期に吸収される光の強度には、以下の関係があります。

ここで、αは動脈血中の光の吸収率、d2はPPG信号のAC成分の振幅です。Idiastoleは、図3においてd1というラベルを付加したDC成分に相当します。式(3)を変形すると、以下のようになります。

ここでは、AC << DCの関係を使っています。


図3. 身体の組織による光の減衰
PPG信号のAC成分とDC成分を算出することで、動脈血中の光の吸収量の変化である-α.d2を求めることができます。この値は、心臓から血液が送り出されることによって生じるものです。その他の組織からは何も影響は受けません。
AC成分とDC成分の比は、灌流指標(PI:Perfusion Index)として知られています。これは、拍動性の血流量と非拍動性の静的な血流量の比だとも言えます。PPGベースの心拍数の計測システムやSpO2の計測システムを設計する際には、次式で表されるAC信号とDC信号の比を大きくすることが目標になります。
PI = AC/DC
赤外光の波長と赤色光の波長におけるPIを使用すれば、PIredとPIirの比である比の比(RoR:Ratio of Ratios)を計算することができます。特定の波長における光の吸収量は、次式のRに比例します。

理論上は、RoRを次式に代入することで、SpO2を計算することができます。
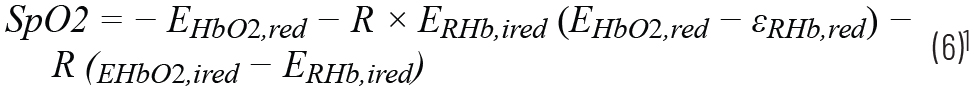
ここで、EHbO2,redは600nmの波長におけるHbO2の吸光係数、EHbO2,iredは940nmの波長におけるHbO2の吸光係数、ERHb,iredは940nmの波長におけるRHbの吸光係数、ERHb,redは600nmの波長におけるRHbの吸光係数です。
但し、ランベルト‐ベールの法則を直接適用することはできません。なぜなら、すべての光学設計には多くの変動要素があり、それらがRoRとSpO2の関係に変化をもたらすからです。変動要素としては、隔壁の機械的な設計、LEDとPDの間隔、電子的/機械的な方法による周辺光の除去量、PDのゲイン誤差などが挙げられます。
PPGベースのパルス・オキシメータにおいて医療グレードの精度を達成するためには、RoRとSpO2の関係を表すルックアップ・テーブルまたはアルゴリズムを開発しなければなりません。
キャリブレーション
SpO2の計測に使用する高精度のアルゴリズムを開発するためには、計測システムのキャリブレーションが必要になります。キャリブレーションを行うためには、次のような学習プロセスが必要になります。そのプロセスでは、医療の専門家によって被験者のSpO2を医学的に低下させるということが行われます。その上で、同専門家による監視と監督が行われます。このようなプロセスは、低酸素研究(Hypoxia Study)として知られています。
SpO2の計測システムでは、リファレンスと同程度の精度を実現する必要があります。リファレンスの選択肢としては、指先にクリップを装着して計測を行う医療グレードのパルス・オキシメータ、絶対的な基準となるCOオキシメータなどがあります。COオキシメータは、血液の酸素飽和度を測定するための侵襲的な方法です。高い精度が得られますが、ほとんどの場合、管理に手間がかかります。
キャリブレーションのプロセスでは、SpO2向けの光学的な計測システムで算出したRoRの値の最良な近似曲線を作成します。その近似曲線は、COオキシメータによるSaO2の測定値を基にして生成します。その近似曲線を使用し、SpO2を計算するためのルックアップ・テーブル(または式)を作成します。
キャリブレーションは、SpO2の計測システムの設計において不可欠な要素です。RoRは、LEDの波長/強度、PDの応答特性、身体の姿勢、周辺光の除去など多くの変数に依存し、設計ごとに異なるからです。
PIが高まり、赤色光/赤外光の波長におけるACのダイナミック・レンジが広くなると、RoRの計算の感度が向上し、SpO2の計測結果としてより正確な値が得られるようになります。
低酸素研究では、SpO2が100%~70%の範囲対象として一定の間隔で計200回の計測を行い、結果を記録する必要があります。被験者は、様々な人種の人を対象とし、年齢と性別が均等に分散するように選択します。このように人種、年齢、性別に多様性を持たせることで、PIに対する個人差の影響を軽減します。
透過型のパルス・オキシメータでは、トータルの誤差を3.0%以下に抑える必要があります。反射型の構成では、誤差を3.5%以下に抑えなければなりません。
設計時に考慮すべき事柄
続いて、SpO2の計測システムを設計する際に考慮すべき事柄について説明します。
透過型か、反射型か
LEDとPDの組み合わせ方としては、透過型の構成と反射型の構成の2つがあります(図4)。どちらの構成でも、PPG信号を取得することができます。透過型の構成では、身体の一部を透過した光(吸収されなかった光)を測定します。この構成は、指や耳たぶなどで測定を行う場合に最適です。それらの部位は毛細血管の密度が高いので、計測上のメリットが得られます。すなわち、測定値の安定性と再現性が高くなり、姿勢の変動の影響を受けにくくなります。結果として、透過型の構成ではPIが40dB~60dB向上します。
一方、反射型の構成は、手首や胸部に装着する機器で使われます。つまり、LEDとPDを隣り合わせで配置しなければならない場合に選択します。


図4. LEDとPDの構成
センサーの装着場所とPI
手首や胸部に装着する機器を開発する場合、AFEにはより広いダイナミック・レンジが求められます。なぜなら、動脈は皮膚、脂肪、骨など、光を反射する要素の下の深い位置に存在するため、DC成分が非常に大きくなるからです。
PPGによる測定の分解能が高いほど、SpO2向けのアルゴリズムの不確実性が低減されます。手首に装着するタイプの機器の場合、SpO2用のセンサーの標準的なPIは1%~2%です。そのため、パルス・オキシメータを設計する際には、機械的な設計によってPIを高めるかダイナミック・レンジを広げることが目標になります。
LEDとPDの間隔は、PIに大きな影響を及ぼします。間隔が狭すぎると、LEDからPDへのクロストークや後方散乱が増大します。それらはDC成分として現れ、AFEが飽和することにつながります。
LEDとPDの間隔を広げれば、クロストークと後方散乱の両方の影響が減少します。しかし、LEDの出力とPDのリターン電流の比である電流伝達率(CTR)も低下します。このことは、PPGベースの計測システムの効率に影響を及ぼします。また、AFEのダイナミック・レンジを最大化するためには、LED用により多くの電力が必要になります。
1個または複数個のLEDを高速かつパルス状に発光させると、信号に対する1/fノイズの影響を低減できるというメリットが得られます。また、LEDをパルス状に発光させることにより、受信側で同期変調を使用して周辺光による干渉を相殺することも可能になります。加えて、複数のパルスを積分するとPD信号の振幅が大きくなり、平均消費電流を下げることができます。更に、PDの総面積を増加させるとより多くの反射光を取り込むことが可能になり、CTRも増加します。
PPGをベースとする心拍数の計測システムについては、単一の大型PDと電力効率の高い複数の緑色LEDの組み合わせがよく使われます。その目的は、血流が制限される場所で計測システムを使用できるようにすることです。緑色LEDを使う理由は、モーション・アーティファクトの除去率が高いからです2。但し、これには消費電力の増加という代償が伴います。緑色LEDは赤色LEDや赤外光LEDよりも順方向電圧が高く、その光は人体の組織における吸光度が高いという特徴があります。したがって、心臓について意味のある情報を得るためには、LEDでより多くの電力を費やす必要があります。
SpO2の計測には、複数種の波長が必要です。また、PPGによる心拍数(HR:Heart Rate)の計測システムでは、ほとんどの場合、効率の高い緑色LEDを採用しています。そのため、PPGベースのHR/SpO2計測システムについては、図5のような構成が最も一般的なものになります。図5のシステムは、アナログ・デバイセズが開発したVSMウォッチです。このシステムでは、緑色/赤色/赤外光LEDのアレイの周囲に複数のPDを配置しています。PDとLEDの間隔は、後方散乱を低減するように最適化されています。また、隔壁の設計によってLEDからPDへのクロストークを低減しています。
当社は、VSMウォッチの試作品を複数使用し、PPGベースのHR/SpO2の計測において最も高い効率が得られるPDとLEDの間隔を導き出しました。


図5. アナログ・デバイセズのVSMウォッチ。HR/SpO2計測システムの最も一般的な構成を採用しています。
モーション・アーティファクトの除去
モーション・アーティファクトは、PPGベースの計測システムを設計する際の大きな課題の1つです。体動が生じた際には、圧力によって動脈と静脈の幅が変化します。すると、PDによって吸収される光の量も変動します。その影響がPPG信号に現れます。身体が静止しているときと比べて、フォトンの吸収量や反射量が変化するということです。
ここでは、無限に幅の広いPD領域によって、無限に長い深部組織のサンプルをカバーすると仮定しましょう。その場合、最終的にすべてのフォトンはPDに向かって反射されます。そうすると、体動によるアーティファクトは検出されません。しかし、これは実現不可能な話です。現実的な解決策は、容量について考慮しつつ、PDの面積を増加させることです。そうすることでAFEのゲインを下げて、モーション・アーティファクトに対するフィルタ処理を行います。
通常、PPG信号の周波数は0.5Hz~5Hzです。それに対し、モーション・アーティファクトの周波数は0.01Hz~10Hzほどです。そのため、単純なバンドパス・フィルタ処理では、PPG信号からモーション・アーティファクトを除去することはできません。体動の影響を高い精度でキャンセルするためには、適応型のフィルタに対して高精度の体動データを供給する必要があります。このような用途に向けて、アナログ・デバイセズは3軸加速度センサー「ADXL362」を開発しました。この製品は、最大8gの測定範囲、1mgの分解能に対応しています。また、出力データ・レートが100Hzの場合でわずか3.6µWしか電力を消費しません。パッケージのサイズは3mm×3mmです。
ADPD4100:アナログ・デバイセズのソリューション
パルス・オキシメータを設計する際には、その装着場所に応じていくつかの課題に直面します。手首に装着するタイプの場合、設計上の課題がより多くなります。対象となるAC信号は、PDで受けた全光量のうちわずか1%~2%にすぎないからです。医療グレードの認証を取得し、HbO2の濃度のわずかな変動を識別できるようにするためには、AC信号に対するダイナミック・レンジを広げる必要があります。これは、周辺光からの干渉を抑え、LEDドライバとAFEのノイズを低減することによって実現できます。ADPD4100は、そうした問題に対処可能な製品です(図6)。
ADPD4100/ADPD4101は、最大100dBのS/N比を達成します。それによって得られるダイナミック・レンジの向上は、PIの低い状況においてSpO2を計測する上で不可欠です。これらのAFEは、低ノイズの電流源とPD入力をそれぞれ8つ備えています。デジタル・タイミング・コントローラは、プログラムが可能な12のタイム・スロットに対応しています。これを使うことで、特定のLED電流、アナログ/デジタルのフィルタ処理、積分オプション、タイミング上の制約を考慮しつつ、PDとLEDに関する一連のシーケンスを定義することができます。
ADPD4100の特徴の1つは、消費電力あたりのS/N比が高いことです。これは、バッテリ駆動の機器によって連続的にモニタリングを実施したい場合に重要なパラメータになります。このような用途を想定し、ADPD4100ではダイナミック・レンジを高めつつ、消費電流を抑えています。ADPD4100は、25Hzの周波数でPPGによる測定を連続的に行う場合、LEDへの給電を含めてわずか30µWの消費電力で75dBのS/N比を達成します。サンプルあたりのパルス数(n)を増やせばS/N比(√n)は向上します。また、LEDの駆動電流を増やすと、それに比例してS/N比が高まります。システムの総消費電力が1µW、LEDの電源が4Vという条件でPPGによる測定を連続的に行う場合、93dBのS/N比が得られます。
ADPD4100は、周辺光を自動的に除去する機能を備えています。それにより、60dBの周辺光除去性能が得られます。また、ホストとなるマイクロプロセッサの負担を軽減することが可能になります。この機能では、1マイクロ秒という高速のLEDパルスをバンドパス・フィルタと共に使用して干渉を除去します。同ICは、特定の動作モードにおいて、LEDがオフの状態におけるPDの暗電流を自動的に算出します。A/Dコンバータで変換を行う前に、LEDがオンの状態の値から暗電流の算出結果を差し引くことによって、周辺光の成分、PDのゲイン誤差/ドリフトを除去することができます。
アナログ・デバイセズは、ADPD4100の評価作業をサポートするものとして、ウェアラブル評価キット「EVAL-ADPD4100-4101」と学習用のVSMウォッチを提供しています。これらは、アナログ・デバイセズの「Wavetool」というアプリケーションとシームレスに接続することが可能です。それにより、生体インピーダンス、心電図、心拍数、SpO2を、複数の波長に対応するPPGベースの手法で測定するシステムの開発を加速することができます(図7)。
学習用のVSMウォッチには、ADPD4100向けの自動ゲイン制御(AGC)のアルゴリズムが組み込まれています。それにより、トランスインピーダンス・アンプのゲインとLEDの電流を調整し、使用するすべてのLEDの波長に対応した最適なAC信号のダイナミック・レンジを得ることができます。


図6. ADPD410Xのブロック図


図7. ADPD4100によるPPGベースの測定結果。赤色LED(右)、赤外光LED(左)を対象として同時測定を行った結果です。
アナログ・デバイセズの別のソリューション
指先や耳たぶに機器を装着してSpO2を計測する場合、手首や胸部に装着する場合よりもS/N比が高くなります。また、指先や耳たぶには骨や組織が少なく、DC成分の影響が減少します。そのため、計測システムの設計は容易だと言えます。
このようなアプリケーションには、光学センサー・モジュール「ADPD144RI」や測光用フロント・エンド「ADPD1080」が適しています。
ADPD144RIは、波長が660nmの赤色LED、同880nmの赤外光LED、4個のPDを2.8mm×5.0mmのパッケージに統合した完全なモジュール製品です。LEDとPDの間隔は、PPGによるSpO2の高精度な計測に向けて最高のS/N比が得られるように最適化されています。このモジュールを採用すれば、LEDとPDの配置や間隔に伴う設計上の課題が解消され、最適な電力対ノイズ比を達成することができます。また同モジュールは、光学的なクロストークを可能な限り低減するよう機械的に最適化されています。そのため、1枚のガラス窓の裏側にセンサーを配置した場合でも、強固なソリューションを実現することができます。
一方のADPD1080は、LEDの駆動用チャンネルを3つ、PDの電流入力用チャンネルを2つ搭載したAFEです。パッケージは2.5mm×1.4mmの17ピンWLCSPを採用しています。このAFEは、基板面積が重視されるチャンネル数の少ないカスタム設計のPPGシステムに適しています。